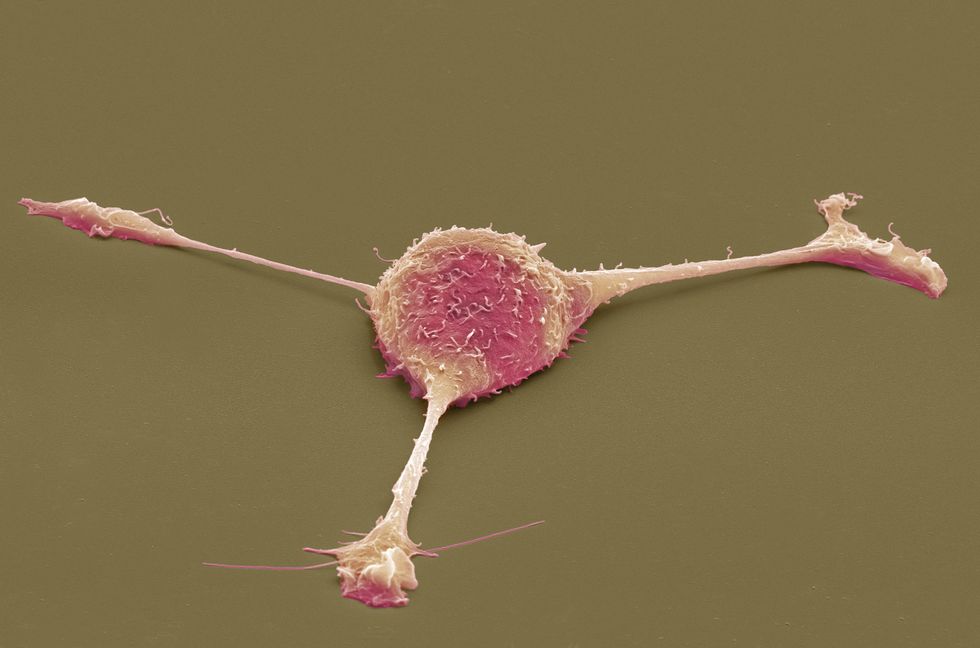
約10年前、実験室で牛の幹細胞から培養された肉を使ったビーフバーガーが初めて調理され、本物の牛肉を一切使わないというこの画期的な 「培養肉」バーガーのトピックスは、各ニュースの見出しを飾りました。
このバーガーのお値段は実に21万7000ポンド(当時のレートで約3200万円)にもなりましたが、それ以降、100社以上の新興企業が牛肉だけでなく鶏肉、豚肉、魚の完全な培養肉の生産に挑戦するようになりました。
そのうちの1社が、BELIEVER Meats(本社イスラエル・レホボト)です。食肉用の家畜を飼育するには膨大な広さの土地と多くの飼料および水を必要とし、温室効果ガス排出の大きな原因にもなっています。そのため、「培養肉製品は動物への残虐性がなく、従来の家畜肉よりも環境に良い」というのが同社の宣伝文句となっています。2018年創業の同社は2022年に、米ノースカロライナ州ウィルソンにて世界最大の培養肉工場の建設を着工しました。BELIEVER Meatsと米培養肉企業Upside Foodsは、高級レストランの限定的な数の顧客に提供するのに十分な肉を培養し、生産することが可能な段階にまで至っています。
培養肉製造の科学技術について、さらに詳しく知るために今回、動物細胞の培養を専門とするノースカロライナ州立大学のポール・モジアック教授(生理学)に話をうかがいました。
以下のインタビュー内容はよりわかりやすく簡潔にするため、若干の編集が施されています。
ポール・モジアック教授:一部の人にとっては、「非難すべきことに見える」とは思っています。ですが、これまでのところ培養肉を食べることに嫌悪感を示した人を私は見たことがありません。私はこれまで培養肉をふるまったことがありますし、調理して食べたことも、生で食べたこともあります。
私の経験から言うと、培養肉の味は普通の食肉と似ていて、本物の肉と大きく違っている点は思いつきません。肉としての食感もあり、とても柔らかくて、風味もまんざらでもない。ただ、タルタルほどではありませんが、とても柔らかいため確かにステーキのような食べ応えはありませんが…。
私たちが牛肉や鶏肉を食べるとき、そのほとんどの場合は「筋繊維を食べている」ことになります。つまりは筋線維になります。それは多核細胞で、その直径は10 ~ 100ミクロンほど。そして、それらの核は有糸分裂後なので分裂して新しい細胞を作成しません。つまり、細胞小器官(DNAを保存する核など、特殊な機能を持つ細胞内の部分)を構成する筋原線維タンパク質ということになります。
市販の「カニかま」は味も食感もカニ肉に似ていますが、実際のカニの身ではありません。基本的に筋タンパク質を全て抽出し、再形成するのです。初期の培養肉製品の多くは、そのようなものになるでしょう。
究極の理想は、例えば実物そっくりの培養肉Tボーンステーキになるようなscaffold(スキャフォールド=培養における足場)を用いることです。そう設計された足場を用意し、その上で十分な厚みが出るようにし、さらにちょうどよい食感になるよう、適切な脂肪バランスになるよう調整することなど、多くの技術上の課題があります。現在わかっていることは、「おいしい製品をつくることは可能な範囲」ということです。
(培養方法を公開している)ほとんどの企業では、線維芽細胞から培養しています。
動物の筋肉は、「筋外膜」と呼ばれる結合組織でまわりを覆われています。その中に、個々の筋肉細胞が束になった筋繊維束があり、それぞれが筋周膜と呼ばれる結合組織層で囲まれています。筋肉を断面図で見てみると、各筋繊維の直径は10~100ミクロンで、細胞としては大きめです。筋繊維には筋肉を動かすためのタンパク質が含まれており、これら全ての層の中に線維芽細胞があります。この細胞は、結合組織のコラーゲンを構成するタンパク質を分泌するものです。
この細胞は、さまざまな種類の細胞やプラットフォームが使用可能です。それは、多様なアプローチ方法があるということ。(筋再生において重要な役割を担っていると考えられている骨格筋を形成する幹細胞)「筋衛星細胞」というプラットフォームを使うのであれば、筋肉からサンプルを採取して粉砕し、増殖する細胞…つまりは筋衛星細胞(筋芽細胞)だけを残します。それを培養皿に入れて増殖させるのです。
また、受精卵の一段階である胚盤胞から取り出した内部細胞塊から単離された細胞「胚性幹細胞」を扱う場合は、胚盤胞から細胞を取り出して増殖させます。前出のBELIEVER Meatsが実施したのは、鶏の皮膚片から皮膚線維芽細胞を採取する方法でした。同社はニワトリの細胞を採取し、皮膚下組織を掻き取って、それを少量の酵素で処理し、培養皿に入れました。その後培養を続け観察していたところ、無限に増殖する細胞を発見したのです。
それは違います。培養肉でも病原菌の心配はあります。食肉を培養するプロセスにはいくつかのポイントで失敗のリスクがあり、最終製品の培養肉にも問題が生じる可能性があります。バイオリアクター(生物反応槽=微生物や酵素を触媒とした、物質の合成や分解、生成を行う装置)内にウイルスが入り、細胞とともに増殖してしまう恐れもあります。例えば、バクテリアをリアクターに入れた場合、通常はバクテリアの増殖スピードの方が培養細胞を上回るため、動物細胞の培養液ではなくバクテリアの培養液になってしまう危険性もあるのです。
リアクターの「フラッシング(洗い流し)」後も、動物肉と同様に被ばく(細菌やウイルスにさらされること)のリスクがあります。動物には消化管があるため、食肉処理の現場にはあらゆる種類の細菌が存在します。培養肉にはそのような問題はありませんが、主なリスクは原料を扱う人間によるものになるのです。そのため、リスクは若干軽減されるものの、完璧に無菌だと考えることはできません。
バイオリアクターの工程終了時に中の細胞塊を取り出し、それを食肉製品にします。私が使っている言葉で言うなら、リアクターのフラッシングとは「ボタンを押すと全内容物がどろどろと底から流れ出ること」になります。その後リアクターを洗浄し、次に使えるよう適切な処理を施す必要があります。
魚の細胞は比較的難しいですね。魚の細胞を培養する場合、細胞が増殖する温度が動物の場合よりも低いのです。つまり、「異なるタイプの培養システムを使う必要がある」ということです。
血液の生理的pHは、血中の二酸化炭素と酸素のバランスによって適切に保たれます。哺乳類やニワトリの細胞と比べると、魚では培地も温度も若干違ってきます。私が常に言っているのは、「細胞培養には繊細な技術が必要とされる」ということです。全てがA+B=Cという公式に当てはまるわけでないのです。なので細胞の培養という点では、この技術の使い手でも、魚の細胞の場合は他の動物の細胞よりもほんの少し扱うのが難しいということになります。
例えばですが、収率(原料の量と実際に取り出した量との割合)40%というのは、「容量1リットルのリアクターから400グラムの培養物が得られる」ということになります。Believer Meatsの場合は、「35%の収率を達成した」と公表していますが、これは本当に素晴らしい成果であり、「この分野を大きく前進させるものだ」と思います。
現在、私たちは無血清の増殖培地で実験し、筋衛星細胞を使用しています。私たちは、ウシES細胞という1990年代に確立された技術を、生物学を解明するために使ってきました。が、これらの方法はまだ実際の量産に向けた応用につながっていません。過去5年間で、より良い収率を大きく達成してはいるのですが…。理論的にわかっていても、人々に食糧を供給するだけの生産工程を導入するとなると難しいのです。
私は鶏肉分野について研究していますが、この場合、胚盤葉の段階から始めることも、ES細胞で研究をしている人から必要なものを入手することもできます。成体動物から組織を採取する必要はないのです。
私ならニワトリのES細胞を採取し、そこから完全に適格な、不活化された細胞バンクをつくり、その細胞バンクの製造プロセスを利用します。この方法のための無血清培地はすでに存在し、バイオ医薬品ですでに使用されています。
ES細胞を使えば、肝細胞をつくることも無理ではないでしょう。ですが通常、肝細胞(肝臓の機能を担う細胞)に分化させるのは、筋細胞よりはるかに難しいことは確かです。それから、肝細胞の風味を出す成分をどうするか? という問題もあります。レバーの風味は非常に強いですから…。
試作版のリアクターの容量は30リットルで、ここから10キロの培養物が取れれば上出来です。工業規模の動物細胞用リアクターの容量は、300~1000リットルであることが多いかと思います。動物細胞用に1000リットルのリアクターを稼動させているバイオ医薬品企業は確かにありますが、(食肉培養目的では)このリアクターの収率は決して良いとは言えません。そもそも目的が違うからです。
もし1000リットルのリアクターを2基並行して稼働させるプラントがあれば、そこから1000キロの培養物が得られるでしょう。ですが、それができるのは月に一度だけになります。食肉処理の世界では、1000キロというのはたいした量ではありません。牛肉処理工場では、その処理に恐らく1時間程度しかかからないでしょう。でも同培養肉の場合は、この量ですと極めて大掛かりなものとなり、手間のかかる作業も必要となります。
とは言え私は、培養肉が流行るときが来ると思っています。問題はそれまでにどれほどの時間、どれほどの資金が必要になるか? ということです。私の職業人生の中で、あるいは私が生きている間にそこまで到達できるのか…。もちろん、私は実現を願っています。
PLEASE FOLLOW US ON INSTAGRAM@エスクァイア日本版
source / POPULAR MECHANICS
Translation / Keiko Tanaka
Edit / Satomi Tanioka
※この翻訳は抄訳です